|
А. Ю. Леин (Институт океанологии им. П. П. Ширшова РАН (ИОРАН)
Опубликовано:"Российский журнал наук о Земле" том 2, N4, Декабрь 2000
|
Содержание
|
Есть основание считать, что синтез СН4 и углеводородов в гидротермальных системах САХ идет по-разному. В осевой циркуляционной гидротермальной системе ТАГ и Брокен Спур основная часть метана флюидов образуется в результате процесса Фишера-Тропша с заметным разделением изотопов углерода 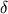 13ССН4 = - 14,6 13ССН4 = - 14,6 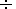 - 18,0 ).В глубинной циркуляционной системе процесс метаногенеза происходит при взаимодействии водорода, образованного при серпентинизации ультрабазитов, с бикарбонатом океанской воды, в присутствии активного Ni-Fe катализатора, который убыстряет процесс синтеза СН4, и тем самым препятствует значительному фракционированию изотопов углерода СН4 по сравнению с углеродом исходного бикарбоната ( - 18,0 ).В глубинной циркуляционной системе процесс метаногенеза происходит при взаимодействии водорода, образованного при серпентинизации ультрабазитов, с бикарбонатом океанской воды, в присутствии активного Ni-Fe катализатора, который убыстряет процесс синтеза СН4, и тем самым препятствует значительному фракционированию изотопов углерода СН4 по сравнению с углеродом исходного бикарбоната ( 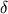 13 С = - 13,4 13 С = - 13,4 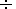 - 14,3, табл. 1). Наличие в сфере реакций СН4, свободного водорода, СО2, воды и металлов - катализаторов синтеза может приводить к образованию сложных молекул углеводородов и их производных, например, по реакции: - 14,3, табл. 1). Наличие в сфере реакций СН4, свободного водорода, СО2, воды и металлов - катализаторов синтеза может приводить к образованию сложных молекул углеводородов и их производных, например, по реакции:
СН4 + СО2 + 2Н2 С2Н5ОН + Н2О . С2Н5ОН + Н2О .
По расчетам О. Г. Сорохтина [Сорохтин, Ушаков, 1991] в рифтовых зонах океана в течение года может образовываться 1800 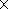 106 т серпентинитов и соответственно 32 106 т серпентинитов и соответственно 32 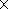 106 т СН4. Результаты моделирования взаимодействия морской воды с толеитовыми базальтами и гарцбургитом также свидетельствуют о возможной генерации большого количества Н2 и СН4. Так, при серпентинизации 1 км 3 гарцбургита может образоваться 5 106 т СН4. Результаты моделирования взаимодействия морской воды с толеитовыми базальтами и гарцбургитом также свидетельствуют о возможной генерации большого количества Н2 и СН4. Так, при серпентинизации 1 км 3 гарцбургита может образоваться 5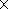 105 т Н2 и 2,5 105 т Н2 и 2,5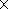 105 т СН4 [Дмитриев и др., 1999]. Часть этих абиогенно синтезированных Н2 и СН4 вместе с Н2S выходят в составе флюидов на поверхность дна, где используются в процессах бактериального хемосинтеза и метанотрофии. Образующаяся при этом биомасса микроорганизмов отличается по изотопному составу серы и углерода от фотосинтезированного ОВ. 105 т СН4 [Дмитриев и др., 1999]. Часть этих абиогенно синтезированных Н2 и СН4 вместе с Н2S выходят в составе флюидов на поверхность дна, где используются в процессах бактериального хемосинтеза и метанотрофии. Образующаяся при этом биомасса микроорганизмов отличается по изотопному составу серы и углерода от фотосинтезированного ОВ.
Сероводород и водород флюидов безусловно полностью утилизируются микрофлорой на активных полях. Этого нельзя сказать с уверенностью о метане, поскольку наблюдаются аномальные концентрации СН 4 в придонных слоях воды на огромных площадях далеко от мест истечения флюидов [Charlou et al., 1998]. Добавим, что СН4 - очень устойчивое соединение и его окисление в биосферных условиях возможно только при участии специфических групп метанокисляющих микроорганизмов. Экспериментальные определения скорости бактериального окисления СН4 в отложениях дна и в водной толще дают, как правило, очень низкие оценки скорости этого процесса [Гальченко и др., 1989; Леин и др., 1993], подтверждая тот факт, что только небольшая часть СН4 гидротермальных флюидов утилизируется метанотрофами, а основная его часть разносится течениями и рассеивается в океане. Следовательно, в водной толще океана, наряду с биогенным, должно присутствовать значительное количество абиогенно синтезированного гидротермального изотопно-тяжелого СН4. По различным оценкам при бактериальных процессах окисления Н2S, Н2 и других восстановленных соединений на активных гидротермальных полях продуцируется около 1% от общего Сорг, образующегося в фотослое океана, и около 50% в среднем от количества Сорг, достигающего дна в рифтовых зонах.
В составе Сорг гидротермальных образований, наряду с бесспорно биогенными липидами, присутствуют сложные многоатомные н-алканы, состав которых не связан напрямую с преобразованием биогенных структур. Содержание таких н-алканов значительно выше в сульфидных рудах из серпентинитовых вмещающих пород. Но и в этих гидротермальных образованиях количество нефтяных углеводородов резко превышает 10% от общего количества Сорг, поэтому пока нет оснований рассматривать абиогенный синтез УВ как существенный источник нефтяных УВ в океане.
Геологический факультет МГУ
|


